Here we are providing Class 10 Science NCERT Solutions in Hindi Chapter – 5 तत्वों के आवर्त वर्गीकरण include all questions presented in the NCERT Science Class 10 books. Candidates can enlist the help of the NCERT Science Class 10 solutions in Hindi on the next page and gain a deeper understanding of the concepts. NCERT Class 10 Science NCERT Solutions in Hindi Chapter – 5 तत्वों के आवर्त वर्गीकरण Class 10 Science NCERT Solutions in Hindi Chapter – 5 तत्वों के आवर्त वर्गीकरण is designed by our team of subject matter experts to help students prepare for exams. Hindi students can view the PDF of the NCERT Class 10 Science Solutions on the page below. From the NCERT Science Book Hindi Questions and Answers on this page, students will learn how to correctly solve NCERT problems.
Remember that the NCERT Class 10 Science Book Solution is the best resource for a good study of the 16 chapters. Use the NCERT Class 10 Science Book Solution as a reference and keep practicing with the answers to questions and exercises until you improve your answers to all chapters of your Class 10 Science Program. Class 10 Science NCERT Solutions in Hindi Chapter – 5 तत्वों के आवर्त वर्गीकरण will help you solve all NCERT Class 10 Science questions chapter 5 smoothly. if you want more notes for various subject then click here
Class 10 Science NCERT Solutions in Hindi Chapter – 5 तत्वों के आवर्त वर्गीकरण
पुष्ठ 91
प्रश्न . कया डॉबेराइनर के त्रिक, न्यूलैंद्स के अष्टक के स्तंभ में भी पाए जाते हैं? तुलना करके पता कीजिए।
उत्तर– हाँ, डॉबेराइनर के त्रिक, न्यूलैंड्स के अष्टक स्तंभ में भी पाए जाते हैं। उदाहरण के लिए लीथियम (Li), सोडियम (Na) तथा पोटाशियम (K) एक डॉबेराइनर का त्रिक बनाते हैं। यदि (la) को पहला तत्व मानें तो उससे आठवें स्थान पर Na आता है और यदि Na को पहला तत्व मानें तो उसके आठवें स्थान परK एटू आता है। इस प्रकार डॉबेराइनर के त्रिक, न्यूलैंड्स के अष्टक स्तंभ में पाए जाते हैं।
प्रश्न 2. डॉबेराइनर के वर्गीकरण की क्या सीमाएं हैं?
उत्तर– डॉबेराइनर के वर्गीकरण की सबसे बड़ी सीमा यह थी कि इस नियम के अनुसार उस समय उपस्थित पाए जाने वाले सारे तत्वों का वर्गीकरण नहीं होता था। ‘उदाहरण–तीन तत्व; नाइट्रोजन (N). फॉस्फोरस (p) तथा ऑरसेनिक (As) के रासायनिक गुणधर्म समान हैं इसलिए इन्हें एक ही त्रिक का होना चाहिए जबकि ह परमाणु ड्रव्यमान (4.0 u), 35 का (74.9uए) तथा 9 का (37.0 u) है जिसके अनुसार यह एक त्रिक के तत्व नहीं हैं। उस समय ज्ञात 30 तत्वों में से 21 तत्वों को त्रिक के रूप में व्यवस्थित नहीं किया जा सका था।
प्रश्न 3. न्यूलैंड्स के अष्टक सिद्धांत की क्या सीमाएं हैं?
उत्तर– (i) अष्टक का सिद्धांत केवल कैल्सियम तक ही लागू होता था, क्योंकि कैल्सियम के बाद प्रत्येक आठवें तत्व का गुणधर्म पहले तत्व से नहीं मिलता।
(ii) न्यूलैंड्स के कल्पना की थी कि प्रकृति में केवल 56 तत्व विद्यमान हैं और भविष्य में कोई अन्य तत्व नहीं मिलेगा। लेकिन, बाद में कई नये तत्व पाए. गये जिनके गुणधर्म, अष्टक सिद्धांत से मेल नहीं खाते थे।
(iii) अपनी सारणी में तत्वों को समंजित करने के लिए न्यूलैंद्स ने दो तत्वों को ‘एक साथ रख दिया था और कुछ असमान तत्वों को एक स्थान में रख दिया था जैसे कोबाल्ट तथा निकैल एक साथ में हैं । इन्हें एक साथ उसी स्तंभ में रखा गया है जिसमें फ्लुओरीन, क्लोरीन एवं ब्रोमीन हैं चाहे इनके गुणधर्म उन तत्वों से भिन्न हैं। आयरन को कोबाल्ट और निकैल से दूर रखा गया है जबकि उनके गुणधर्मों में समानता होती है।
(iv) न्यूलैंड्स अष्टक सिद्धांत केवल हल्के तत्वों के लिए ठीक से लागू हो पाया ह
पृष्ठ 94
प्रश्न 1. मेंडलीफ के आवर्त सारणी का उपयोग कर निम्नलिखित तत्वों के ऑक्साइड के सूत्र का अनुमान कीजिए—K, C, AI, Si, Ba
उत्तर– पोटैशियम (k) वर्ग IA का धातु है। इसकी संयोजकता 1 है। इसलिए इसके ऑक्साइड का सूत्र k O है।
(ii) कार्बन (C) वर्ग IV A का तत्व है। इसकी संयोजकता 4 है तथा इसके ऑक्साइड का सूत्र CO2 है।
(iii) AI वर्ग गा III A का तत्व है। इसकी संयोजकता 3 है। इसलिए इसके ऑक्साइड का सूत्र AI2 O3 है।
(iv) सिलिकॉन (Si) IV A वर्ग का तत्व है। इसकी संयोजकता 4 है। इसलिए इसकी ऑक्साइड का सूत्र SiO2 है।
(v). Ba वर्ग IIA का तत्व है। इसकी संयोजकता 2 है । इसलिए इसकी ऑक्साइड का सूत्र BaO है।
प्रश्न 2. गैलियम के अतिरिक्त, अब तक कौन-कौन से तत्वों का पता चला है जिसके ‘लिए मेंडलीफ ने अपनी आवर्त सारणी में खाली स्थान छोड़ दिया था? दो ‘उदाहरण दीजिए।
उत्तर– जर्मेनियम (Ge) तथा पोलोनियम (90) वर्ग (po) के दो तत्व हैं। इन दोनों तत्वों के लिए भी मेंडलीफ ने अपनी आवर्त सारणी में खाली स्थान छोड़ दिया था। मेंडलीफ ने इनके गुणधर्म पहले से ही बता दिए थे। जब बाद में इन तत्वों की खोज हुई तो इनके गुणधर्म लगभग वही थे जो मेंडलीफ ने दिए थे।
प्रश्न 3. मेंडलीफ ने अपनी आवर्त सारणी तैयार करने के लिए कौन-सा मापदंड.अपनाया था?
उत्तर– मेंडलीफ ने अपनी सारणी में तत्वों को उनके मूल, गुणधर्म, परमाणु द्रव्यमान तथा रासायनिक गुणधर्मों में समानता के आधार पर व्यवस्थित किया। जब मेंडलीफ ने अपना कार्य प्रारंभ किया, तब तक 63 तत्व ज्ञात थे। उन्होंने तत्वों के परमाणु द्रव्यमान और उनके भौतिक तथा रासायनिक गुणधर्मों के बीच संबंधों का अध्ययन किया । रासायनिक गुणधर्मों के अंतर्गत में डलीफ ने तत्वों के ऑक्सीजन एवं हाइड्रोजन के साथ बनने वाले यौगिकों की ओर ध्यान केंद्रित किया। उन्होंने ऑक्सीजन एवं हाइड्रोजन को इसलिए चुनाव किया क्योंकि वे अत्यंत सक्रिय हैं तथा अधिकांश तत्वों के साथ यौगिक बनाते हैं। तत्व से बनने वाले हाइड्राइड एवं ऑक्साइड के सूत्र को तत्वों के वर्गीकरण के लिए मूलभूत गुणधर्म माना गया। फिर उन्होंने 63 कार्ड लिए एवं प्रत्येक कार्ड पर अलग-अलग तत्वों के गुणधर्मों को ‘लिखा। उन्होंने समान गुणधर्म वाले तत्वों को अलग कर दिया तथा इन पत्तों को पिन लगाकर दीवार पर लटका दिया। उन्होंने देखा कि अधिकांश तत्वों को आवर्त सारणी में स्थान मिल गया था तथा अपने परमाणु द्रव्यमान के आरोही क्रम में ये तत्व व्यवस्थित हो गये। यह भी देखा गया कि समान भौतिक एवं रासायनिक गुणधर्म वाले विभिन्न तत्व एक निश्चित अंतर के बाद फिर आ जाते हैं। इसी आधार पर मेंडलीफ ने आवर्त सारणी बनाई।
प्रश्न 4. आपके अनुसार उत्कृष्ट गैसों को अलग समूह में क्यों रखा गया?
उत्तर– सभी तत्वों में से उत्कृष्ट गैसें जैसे-हीलियम (He) निऑन (Ne), आर्गन (Ar) ‘क्रिप्टॉन (Kr) तथा जीनॉन (Xe) सबसे अधिक अक्रियाशील है। इनके गुणधर्म किसी अन्य समूह के तत्वों के समान नहीं है। ये अन्य तत्वों से अभिक्रिया नहीं ‘करते। इसलिए मेंडलीफ ने उन्हें अलग वर्ग में रखा जिसे उसने शुन्य वर्ग कहा।
पृष्ठ 100
प्रश्न 1. आधुनिक आवर्त सारणी दूवारा किस प्रकार से मेंडलीफ की आवर्त सारणी की विविध विसंगतियों को दूर किया गया?
उत्तर– मेंडलीफ की आवर्त सारणी परमाणु द्रव्यमान के सिद्धांत पर आधारित थी जबकि मोसले की आधुनिक आवर्त सारणी परमाणु संख्या पर आधारित है। इस सारणी के ‘दूवारा मेंडलीफ की सारणी के दोषों को दूर किया गया–
(i) आधुनिक आवर्त सारणी में सभी समस्थानिकों को एक ही स्थान दिया गया है क्योंकि समस्थानिकों में प्रोटॉनों की संख्या तो सदा समान होती है इसलिए परमाणु संख्या भी एक समान ही होगी।
(ii) आरगॉन तथा पोयशियम की परमाणु संख्या क्रमश: 18 और 19 हैं। तत्वों की बढ़ती परमाणु संख्या के आधार पर व्यवस्थित करने पर ऑरगान पहले आ जाता है और पोटाशियम का स्थान पीछे रह जाता है जबकि उनके परमाणु द्रव्यमान इसके विपरीत हैं । नई आवर्त सारणी में इस दोष को दूर किया गया है।
(iii) तत्वों, उत्कृष्ट गैसों और संक्रमण तत्वों को स्पष्ट रूप से अलग-अलग किया गया है।
(iv) आधुनिक आवर्त सारणी स्पष्ट रूप से दर्शाती है कि तत्वों के गुणों की ‘पुनरावृत्ति क्यों होती है।
(v) हाइड्रोजन को प्रथम ग्रुप के ऊपर विशेष स्थान दिया गया जो उसके गुणों और इलैक्ट्रॉनिक विन्यास के आधार पर किया गया है। ं
प्रश्न 2. मैग्नीशियम की तरह रासायनिक अभिक्रियाशीलता दिखाने वाले दो तत्वों के नाम लिखिए। आपके चयन का क्या आधार है?
उत्तर– आधुनिक आवर्त सारणी के अनुसार, जिन तत्वों की बाहरी इलैक्ट्रॉनिक विन्यास समान होती है उनके गुणधर्म भी समान होते हैं। मैग्नीशियम के बाहरी कक्ष या कोश में दो इलैक्ट्रॉन हैं इसलिए वे सभी तत्व जिनके बाहरी कोश में 2 इलैक्ट्रॉन होंगे वह Mg के समान ही गुणधर्म प्रदर्शित करेंगे।
‘उदाहरण– कैल्सियम (Ca) परमाणु संख्या = 20
कक्ष में व्यवस्थित इलैक्ट्रॉन → 2, 8, 8, 2
मैग्नीशियम (Mg), परमाणु संख्या = 12
कक्ष में व्यवस्थित इलैक्ट्रॉन → 2, 8, 2
प्रश्न 3. निम्न के नाम बताइए–
(a) तीन तत्वों जिनके सबसे बाहरी कोश में एक इलैक्ट्रॉन उपस्थित हो।
(b) दो तत्वों जिनके सबसे बाहरी कोश में दो इलैक्ट्रॉन उपस्थित हों।
(c) तीन तत्वों जिनका बाहरी कोश पूर्ण हो।
उत्तर—
(a) तीन तत्व जिनके सबसे बाहरी कोश में एक इलैक्ट्रॉन उपस्थित है । उदाहरण है- |
(b) दो तत्व जिनके बाहरी कोश में 2 इलैक्ट्रॉन हैं । उदाहरण हैं–
(c) ऐसे तीन तत्व जिनका बाहरी कक्ष/कोश पूर्ण हैं । उदाहरण हैं–
प्रश्न 4. . (a) लीथियम, सोडियम, पोटैशियम यह सभी धातुएं जल से अभिक्रिया कर हाइड्रोजन गैस मुक्त करती हैं। क्या इन तत्वों के परमाणुओं मे कोई समानता है?
(b) हीलियम एक अक्रियाशील गैस है जबकि निऑन की अभिक्रियाशीलता अत्यंत कम है। इनके परमाणुओं में कोई समानता है?
उत्तर—
(a) लीथियम, सोडियम तथा पोटैशियम की जल के साथ अभिक्रिया–
(b) He तथा Ne दोनों ही उत्कृष्ट गैसें हैं इसलिए ये अक्रियाशील हैं। इनके बाहरी कोश पूर्ण हैं । He के पास केवल K कोश है और यह पूर्ण है पर दूसरी तरफ Ne के पास K तथा L दो कोश हैं और ये दोनों भी पूर्ण हैं । कोश के पास दो तथा L कोश के पास आठ इलैक्ट्रॉन हैं ।
इसलिए निऑन की अभिक्रियाशीलता अत्यंत कम है।
प्रश्न 5. आधुनिक आवर्त सारणी के पहले दस तत्वों में कौन-से धातु हैं?
उत्तर– पहले दस तत्व हैं– H, He, Li, Be, B, C, N, O, F तथा Ne इन सब तत्वों में से धातु हैं– Li तथा Be
प्रश्न 6. आवर्त सारणी में इनके स्थान के आधार पर इनमें से किस तत्व में सबसे अधिक धात्विक अभिलक्षण की विशेषता है?
Ga, Ge, As, Se, Be
उत्तर– पहले इनका वर्गीकरण बढ़ती हुई परमाणु संख्या के अनुसार करते हैं–
हम जानते हैं कि धात्विक अभिलक्षण स्तंभ में बाएँ से दाएँ तरफ कम होता है तथा वर्ग में नीचे जाते समय बढ़ता है। इस बात को ध्यान में रखते हुए Be तथा Ga का धात्विक अभिलक्षण ज़्यादा लगता है। पर Ga जल्दी अपने इलैक्ट्रॉन दे सकता है इसलिए Ca, Be से ज़्यादा धात्विक है।
NCERT अभ्यास प्रश्नोत्तर
प्रश्न 1. आवर्त सारणी में बाएँ से दाएँ जाने पर प्रवृत्तियों के बारे में कौन-सा कथन असत्य है?
(a) तत्वों की धात्विक प्रकृति घटती है।
(b) संयोजकता इलैक्ट्रॉनों की संख्या बढ़ जाती है।
(c) परमाणु आसानी से इलैक्ट्रॉन का त्याग करते हैं।
(d) इनके ऑक्साइड अधिक अम्लीय हो जाते हैं।
उत्तर– केवल कथन (C) गलत (असत्य) है क्योंकि आवर्त सारणी में बाएँ से दाएँ जाने पर परमाणु की इलैक्ट्रॉन त्यागने की क्षमता घटती है।
प्रश्न 2. तत्व X, XCL2 सूत्र वाला एक क्लोराइड बनाता है, जो एक ठोस है और जिसका गलनांक अधिक है। आवर्त सारणी में यह तत्व संभवत किस समूह के अंतर्गत होगा?
(a) Na (b) Mg (c) AL (d) Si.
उत्तर– यदि तत्व X , XCL2 सूत्र का क्लोराइड बनाता है तो X तत्व के संयोजक इलैक्ट्रॉन की संख्या 2 होगी अर्थात् उसके बाहयतम कक्ष में संयोजकता इलैक्ट्रॉन की संख्या 2 होगी । आवर्त सारणी के अनुसार केवल वर्ग 2 के तत्व Be, Mg, Ca, Sr, Ba
एवं Ra को संयोजकता इलैक्ट्रॉन संख्या दो है। इसलिए X तत्व Mg (मैग्नीशियम) है क्योंकि मैग्नीशियम एक धातु होते हुए भी एक आयनिक क्लोराइड बनाने की क्षमता रखता है, जिसका उच्च गलनांक हो। अत: कथन (£) सही है।
प्रश्न 3. किस तत्व में –
(a) दो कोश है तथा दोनों इलैक्ट्रॉनों से पूरित हैं।
(b) इलैक्ट्रॉनिक विन्यास 2. 8, 2 है।
(c) कुल तीन कोश हैं तथा संयोजकता कोश में चार इलैक्ट्रॉन हैं ?
(d) कुल दो कोश हैं तथा संयोजकता कोश में तीन इलैक्ट्रॉन हैं ?
(e) दूसरे कोश में पहले कोश से दुगुने इलैक्ट्रॉन हैं ?
उत्तर– (a) उत्कृष्ट गैसों के सभी शैल इलैक्ट्रॉन से भरे होते हैं । इसलिए दिया गया तत्व एक उत्कृष्ट तत्व गैस है। क्योंकि इसके दो पूर्णतः भरे शैल हैं इसलिए यह वर्ग में दो हैं। इस प्रकार तत्व Ne (निऑन) यह तत्व है।
(b) इलैक्ट्रॉनिक विन्यास 2. 8, 2 का जोड़ 12 जो इस तत्व का परमाणु अंक है और12 परमाणु अंक वाला तत्व Mg (मैग्नीशियम) है। अत: दिया गया तत्व Mg (मैग्नीशियम) है।
(c) कुल तीन कोश में से बाहय कोष में इलैक्ट्रॉन की संख्या 4 है। अत: तत्व का इलैक्ट्रॉनिक विन्यास है-2. 8, 4 विन्यास का जोड़ होगा 14, इस प्रकार 14 परमाणु अंक वाला तत्व है– Si (सिलिकॉन) ।
(d) कुल दो कोश हैं बाहय कोश में 3 इलैक्ट्रॉन हैं। इस प्रकार तत्व का इलैक्ट्रॉनिक विन्यास है-2, 3 तथा विन्यास जोड़ है- 5 अत: इलैक्ट्रॉनिक
विन्यास 5 वाला तत्व है B (बोरॉन) ।
(e) दूसरे कोश में पहले की अपेक्षा दुगुने इलैक्ट्रॉन हैं अत: तत्व का इलैक्ट्रॉनिक विन्यास है–2, 4 तथा विन्यास जोड़-6 इस प्रकार परमाणु संख्या 6 वाला तत्व है- C (कार्बन) ।
प्रश्न 4. (a) आवर्त सारणी में बोरॉन के स्तंभ के सभी तत्वों के कौन-से गुणधर्म समान हैं ?
(b) आवर्त सारणी में फ्लुओरीन के स्तंभ के सभी तत्वों के कौन-से गुणधर्म समान हैं?
उत्तर– (a) आवर्त सारणी में बोरॉन स्तंभ के सभी तत्व 13 से संबंध रखते हैं। इसलिए इन सबके बाहयतम संयोजकता कोश में इलैक्ट्रॉन की संख्या तोन (3) होगी। केवल बोरॉन (B) को छोड़कर क्योंकि यह एक अधातु है और शेष तत्व धातुएं हैं, जैसे-AI, Ga, In और Th
(b) फ्लुओरीन के स्तंभ में आने वाले सभी तत्व उत्कृष्ट तत्व हैं तथा वर्ग 17 से संबंध रखते हैं। इसलिए उनके बाहयतम कोश में इलैक्ट्रॉन की संख्या 7 होगी। यह सभी तत्व F, CI, Br, I अधातुएँ हैं।
प्रश्न 5. एक परमाणु का इलैक्ट्रॉनिक विन्यास 2, 8, 7 है।
(a) इस तत्व की परमाणु-संख्या क्या है?
(b) निम्न में से किस तत्व के साथ इसकी रासायनिक समानता होगी?
(परमाणु-संख्या कोष्ठक में दी गई है ) N(7), F(9), P(15), Ar(18)
उत्तर– (a) तत्व की परमाणु संख्या/परमाणु अंक 2 + 8 + 7 = 17 है और यह तत्व क्लोरीन है।
(b) क्योंकि तत्व के बाहयतम संयोजकता कोश में इलैक्ट्रॉन की संख्या 7 है इसलिए यह उत्कृष्ट तत्वों के वर्ग 17 से संबंध रखता है। इस परिवार के अन्य तत्वों की परमाणु संख्या एवं इलैक्ट्रॉनिक विन्यास है।
|
तत्व |
परमाणु संख्या |
इलैक्ट्रॉनिक विन्यास |
|
फ्लोरिन |
9 |
2,7 |
|
ब्रोमीन |
35 |
2,8,18,7 |
|
आयोडीन |
53 |
2,8,18,18,7 |
इस प्रकार तत्व F परमाणु संख्या 9 के कारण उत्कृष्ट तत्वों के परिवार से संबंध ‘रखता है। इसलिए यह तत्व क्लोरीन तत्व से रासायनिक रूप से समान होगा।
प्रश्न 6. आवर्त सारणी में तीन तत्व A, B तथा C की स्थिति निम्न प्रकार है—
|
समूह 16 |
समूह 17 |
|
– |
– |
|
– |
A |
|
– |
– |
|
B |
C |
अब बताइए कि–
(a) A धातु है या अधातु।
(b) A की अपेक्षा ( अधिक अभिक्रियाशील है या कम?
(c) C का आकार छ से बड़ा होगा या छोटा ?
(d) तत्व A, किस प्रकार के आयन, धनायन या ऋणायन बनाएगा?
उत्तर- (a) समूह 17 के तत्वों के बाहयतम संयोजकता कोश में इलैक्ट्रॉन की संख्या 7 है और सभी तत्व एक इलैक्ट्रॉन धारण करने की उच्च क्षमता रखते हैं । अतः सभी तत्व अधातु हैं।
(b) एक वर्ग में नीचे की ओर आने पर परमाणु आकार बढ़ता है। इसलिए नाभिक की बाहयतम इलैक्ट्रॉन को खींचने की क्षमता कम हो जाती है। इस प्रकार अभिक्रियाशीलता एक वर्ग में नीचे आने पर कम हो जाती है। इसलिए तत्व C तत्व A से कम अभिक्रियाशील है।
(C) तत्व B एवं C समान आवर्तित (Period) से संबंध रखते हैं।
प्रश्न 7. नाइट्रोजन ( परमाणु संख्या 7) तथा फॉस्फोरस ( परमाणु संख्या 15) आवर्त सारणी के समूह 5 के तत्व हैं। इन दोनों तत्वों का इलैक्ट्रॉनिक विन्यास लिखिए। इनमें से कौन-सा तत्व अधिक ऋण विद्युत् होगा और क्यों ?
उत्तर– नाइट्रोजन तथा फॉस्फोरस की इलैक्ट्रॉनिक विन्यास हैं-
ये दोनों तत्व आवर्त सारणी के बायीं से दायीं ओर स्थित हैं । इसलिए वे अधातु की श्रेणी में आते हैं। ये धातु नहीं है।
प्रश्न 8. तत्वों के इलैक्ट्रॉनिक विन्यास का आधुनिक आवर्त सारणी में तत्व की स्थिति से कया संबंध है?
उत्तर– यदि
तत्व का इलैक्ट्रॉनिक विन्यास ज्ञात हो तो आवर्त सारणी में उसकी स्थिति को
ज्ञात किया जा सकता है,
इसके विपरीत यदि आवर्त सारणी में तत्व की स्थिति का
ज्ञान हो तो उसका इलैक्ट्रॉनिक विन्यास ज्ञात किया जा सकता
है। उदाहरण के लिए, यदि एक तत्व का स्तंभ 3 एवं वर्ग 15 से संबंधित है तथा उसके बाहयतम संयोजकता कक्ष में इलैक्ट्रॉन की संख्या 5 है क्योंकि यह तत्व स्तंभ 3 से संबंधित
है, इसलिए इसका बाहयतम संयोजकता कक्ष M होगा तथा इसका इलैक्ट्रॉनिक ‘विन्यास होगा- (K L M) ,(2 8 5) हो जैसे— (K L M, N,)(2 8 18 7)
क्योंकि तत्व के संयोजकता इलैक्ट्रॉन 7 है। इसलिए यह वर्ग 17 से संबंधित है। (10 + 7) क्योंकि संयोजकता कक्ष चौथा कक्ष है, इसलिए तत्व स्तंभ 4 से संबंधित है अर्थात् यह तत्व ब्रोमीन (Br) है।
प्रश्न 9. आधुनिक आवर्त सारणी में कैल्सियम ( परमाणु संख्या 20) के चारों ओर 12, 19, 21 तथा 38 परमाणु-संख्या वाले तत्व स्थित हैं। इनमें से किन तत्वों के भौतिक एवं रासायनिक गुणधर्म कैल्सियम के समान है?
उत्तर– आवर्त सारणी का एक तत्व जो अन्य 4 (चार) तत्वों से घिरा हो वह उन सबका केंद्रीय भाग कहलाएगा। दिए गए तत्वों को यदि इस प्रकार लिखा जाए
दिए गए ढांचे में तत्व कैल्सियम (परमाणु संख्या – 20) अन्य 4 तत्वों (परमाणु संख्या क्रमश: 12, 19, 21 एवं 38) । इस प्रकार एक ही वर्ग में आने वाले तत्वों के परमाणु संख्या है-12, 20 एवं 38, अत: केवल तत्व (परमाणु संख्या ) 12, 38) के भौतिक एवं रासायनिक गुणधर्म कैल्सियम के समान हैं ।
प्रश्न 0. आधुनिक आवर्त सारणी एवं मेंडलीफ की आवर्त सारणी में तत्वों की व्यवस्था की तुलना कीजिए।
उत्तर– मेंडलीफ की आवर्त सारणी की आवर्त सारणी के दीर्घ रूप से तुलना-मेंडलीफ की आवर्त सारणी और आधुनिक आवर्त सारणी में तत्वों को एक समान तालिका के रूप में स्थान दिया गया है । दोनों सारणियों में एक समान गुणों वाले तत्वों को एक ही ग्रुप में रखा गया है लेकिन इन दोनों में काफ़ी समानताएँ हैं; जैसे-
|
मेंडलीफ की आवर्त सारणी |
आधुनिक आवर्त सारणी |
|
1. उस समय तक ज्ञात 63 तत्वों को बढ़ ते परमाणु द्रव्यमानों में व्यवस्थित किया गया था। 2. इस आवर्त सारणी में 8 ऊर्ध्वाधर स्तंभ हैं, जिन्हें वर्ग कहते हैं । 3. तत्वों के समस्थानिकों को सारणी में स्थान नहीं मिल सका। 4. रासायनिक दृष्टि से असमान तत्वों को भी एक साथ रखा गया था। 5. सभी संक्रमण तत्वों को एक ही वर्ग VIII पता में रखा गया। 6. उत्कृष्ट गैसों की इस सारणी के बनने तक खोज ही नहीं हो पाई थी। 7. कुछ उच्च द्रव्यमान वाले तत्वों को उन तत्वों से पहले स्थान दिया गया जिनका परमाणु द्रव्यमान कम है। |
1. कुल 118 तत्वों को बढ़ते परमाणु क्रमांक में व्यवस्थित किया गया है। 2. इसमें1 8 ऊर्ध्वाधर स्तंभ हैं जिन्हें वर्ग कहते हैं तथा 7 आवर्त हैं । 3. तत्वों के समस्थानिकों को सारणी में उचित स्थान प्राप्त हुआ क्योंकि उनके परमाणु क्रमांक एक-समान होते हैं। 4. रासायनिक दृष्टि से असमान तत्वों को अलग-अलग वर्गों में स्थान दिया गया। 5. संक्रमण तत्वों को वर्ग 3 से वर्ग 12 में रखा गया। 6. उत्कृष्ट गैसों को वर्ग 18 में स्थान दिया गया है। 7. इस सारणी में वर्गीकरण का आधार परमाणु क्रमांक है इसलिए इसमें ‘प्रतिलोम क्रम का दोष नहीं है। |
NCERT प्रश्न प्रदर्शिका EXEMPLAR PROBLEMAS
‘बहुविकल्पीय प्रश्न
प्रश्न 1. किस तत्व तक अष्टक का नियम लागू हो पाया
(a) ऑक्सीजन
(b) कैल्सियम
(c) कोबाल्ट
(d) पोटैशियम
Ans:- (b)
प्रश्न 2. मेंडेलीफ आवर्त नियम के अनुसार, आवर्त सारणी में तत्व किस क्रम में व्यवस्थित थे
(a) परमाणु क्रमांक के बढ़ते क्रम में.
(b) परमाणु क्रमांक के घटते क्रम में
(c) परमाणु भार के बढ़ते क्रम में
(d) परमाणु भार के घटते क्रम में
Ans:- (c)
प्रश्न 3. मेंडेलीफ आवर्त सारणी में उन तत्वों के लिए रिक्त स्थान छोड़ दिए गए थे जिनकी खोज बाद में हुईं। निम्नलिखित में से किस तत्व को आवर्त सारणी में बाद में स्थान मिला ?
(a) जर्मेनियम
(b) क्लोरीन
(c) ऑक्सीजन
(d) सिलिकन
Ans:- (a)
प्रश्न 4. आधुनिक आवर्त सारणी के संदर्भ में निम्नलिखित में से कौन-सा/ कौन-से कथन गलत है/हैं?
(i) आधुनिक आवर्त सारणी में तत्वों को उनके घटते हुए परमाणु क्रमांक के आधार पर व्यवस्थित किया है।
(ii) आधुनिक आवर्त सारणी में तत्वों को उनके बढ़ते हुए परमाणु भारों के आधार पर व्यवस्थित किया है।
(iii) आवर्त सारणी में समस्थानिकों को संलग्न समूहों में रखा गया है।
(iv) आधुनिक आवर्त सारणी में तत्वों को उनके परमाणु क्रमांक के बढ़ते हुए क्रम में व्यवस्थित किया है।
(a) केवल (i)
(b), (7) तथा (0)
(c) (i), (ii) तथा (iv)
(d) केवल (iv)
Ans:- (b)
प्रश्न 5. आधुनिक आवर्त सारणी के संदर्भ में कौन-सा कथन सत्य हैं?
(a) इसमें 18 श्षैतिज पंक्तियाँ हैं जिन्हें आवर्त कहते हैं।
(b) इसमें 7 ऊर्ध्वाधर कॉलम हैं जिन्हें आवर्त कहते हैं।
(c) इसमें 18 ऊर्ध्वाधर कॉलम हैं जिन्हें समूह कहते हैं।
(d) इसमें 7 क्षैतिज पंक्तियाँ हैं जिन्हें समूह कहते हैं।
Ans:- (c)
प्रश्न 6. दिए गए तत्वों A, B, C, तथा E ( परमाणु क्रमांक क्रमशः 2, 3, 7, 10 तथा 30 ) में से समान आवर्त से संबंधित तत्व हैं–
(a) A,B,C
(b) B,C,D
(c) A,D,E
(d) B,D,E
Ans:- (b)
प्रश्न 7. तत्व A,B,C,D तथा E के परमाणु क्रमांक क्रमशः 9,11, 17, 12 तथा 13 हैं। तत्वों का कौन-सा युग्म समान समूह से संबंधित है?
(a) A तथा B
(b) B तथा D
(c) A तथा C
(d) D तथा E
Ans:- (c)
प्रश्न 8. आधुनिक आवर्त सारणी में इलेक्ट्रॉनिक विन्यास 2, 8 युक्त तत्व को आप किस समूह में पाते हैं ?
(a) समूह 8
(b) समूह 2
(c) समूह 18
(d) समूह 10
Ans:- (c)
प्रश्न 9. एक तत्व जो सभी कार्बनिक यौगिकों का आवश्यक अवयव है, संबंधित है
(a) समूह । से
(b) समूह 14 से
(c) समूह 15 से
(d) समूह 6 से
Ans:- (b)
प्रश्न 10. आवर्त 2 के तत्वों के लिए निम्नलिखित में से कौन-सा कोश बादह्यतम है?
(a) K कोश
(b) L कोश
(c) M कोश
(d) N कोश
Ans:- (b)
प्रश्न 11. निम्नलिखित में से कौन-सा तत्व अधिकतम संयोजी इलेक्ट्रॉन रखता है?
(a) Na
(b) Al
(c) Si
(d) P
Ans:- (d)
प्रश्न 12. O, प तथा ४ की परमाण्वीय त्रिज्याओं का बढ़ता हुआ सही क्रम निम्नलिखित में से कौन-सा है?
(a) O, F, N
(b) N , F, O
(c) O, N, F
(d) F, O, N
Ans:- (d)
प्रश्न 13. निम्नलिखित में से किस तत्व की परमाण्वीय त्रिज्या सर्वाधिक है ?
(a) Na
(b) Mg
(c)
(d) Ca
Ans:- (c)
प्रश्न 14. निम्नलिखित में से कौन-सा तत्व आसानी से इलेक्ट्रॉन खो देता है?
(a)Mg
(b) Na
(c) K
(d) Ca
Ans:- (c)
प्रश्न 15. निम्नलिखित में से कौन-सा तत्व आसानी से इलेक्ट्रॉन नहीं खोता है?
(a) Na
(b)
(c) Mg
(d) Al
Ans:- (b)
प्रश्न 16. निम्नलिखित में से कौन-से एक तत्व के समस्थानिकों के अभिलक्षण हैं ?
(i) एक तत्व के समस्थानिकों के परमाणु भार समान होते हैं ।
(ii) एक तत्व के समस्थानिकों के परमाणु क्रमांक समान होते हैं ।
(iii) एक तत्व के समस्थानिकों के भौतिक गुण समान होते हैं।
(iv) एक तत्व के समस्थानिक समान रासायनिक गुण प्रदर्शित करते हैं।
(a) (i) (iii) तथा (iv)
(b) (ii), (iii) तथा (iv)
(c) (ii) तथा (iii)
(d)
(ii) तथा (iv)
Ans:- (d)
प्रश्न 17. निम्नलिखित तत्वों को उनके धात्विक गुणों के घटते हुए क्रम में व्यवस्थित कीजिए–
Na, Si, CI, Mg, Al
(a) Cl > Si > AI > Mg > Na
(b) Na > Mg > Al > Si > CI
(c) Na > Al > Mg > Cl > Si
(d)Al > Na > Si > Ca > Mg
Ans:- (b)
प्रश्न 18. निम्नलिखित तत्वों को उनके अधात्विक गुण के बढ़ते हुए क्रम में व्यवस्थित कीजिए–
Li, O, C, Be, F
(a) F < O < C < Be < Li
(b) Li < Be < C < O < F
(c) F < O < C < Be < Li
(d) F < O < Be < C < Li
Ans:- (b)
प्रश्न 19. एका – ऐलुमिनियम किस प्रकार का ऑक्साइड बनाता है?
(a) EO3
(b) E3O2
(c) E2O3
(d) EO
Ans:- (c)
प्रश्न 20. तीन तत्व B, Si, तथा Ge हैं–
(a) धातुएँ
(b) अधातुएँ
(c) उपधातुएँ
(d) क्रमश: धातु, अधातु तथा उपधातु
Ans:- (c)
प्रश्न 21. निम्नलिखित में से कौन-सा तत्व अम्लीय ऑक्साइड बनता है?
(a) परमाणु क्रमांक 7 युक्त तत्व
(b) परमाणु क्रमांक 3 वाला तत्व
(c) परमाणु क्रमांक 12 वाला तत्व
(d) परमाणु क्रमांक 19 वाला तत्व
Ans:- (a)
प्रश्न 22. परमाणु क्रमांक 4 वाला तत्व कठोर है तथा अम्लीय ऑक्साइड एवं एक सहसंयोजक हैलाइड बनाता है। यह तत्व निम्नलिखित में से किस वर्ग से संबंधित है ?
(a) धातु
(b) उपधातु
(c) अधातु
(d) बायीं ओर वाले तत्व
Ans:- (b)
प्रश्न 23. एक परमाणु की परमाण्वीय त्रिज्या का निम्नलिखित में से कौन-सा सही प्रदर्शन है—
(a) (i) तथा (ii)
(b) (ii) तथा (iii)
(c) (iii) तथा (iv)
(d) (i) तथा (iv)
Ans:- (b)
प्रश्न 24. आवर्त सारणी के एक समूह में ऊपर से नीचे जाने पर निम्नलिखित में से कया नहीं बढ़ता है?
(a) परमाण्वीय त्रिज्या
(b) धात्विक लक्षण
(c) संयोजकता
(d) एक तत्व में कोशों की संख्या
Ans:- (c)
प्रश्न 25. आवर्त सारणी के आवर्त में बायें से दायें जाने पर सामान्यतः परमाणु का आकार
(a) बढ़ता है
(b) घटता है
(c) विशेष परिवर्तन नहीं होता है।
(d) पहले घटता है फिर बढ़ता है।
Ans:- (b)
प्रश्न 26. निम्नलिखित में से तत्वों का कौन सा समूह, धात्विक गुणों के बढ़ते हुए क्रम में लिखा गया है?
(a) Be Mg Ca
(b) Na Li K
(c) Mg Al Si
(d) C O N
Ans:- (a)
‘लघुउत्तरीय प्रश्न
प्रश्न 27. समान गुणों वाले तीन तत्वों A, B तथा C के परमाणु भार क्रमशः X, Y तथा Z है। B का परमाणु भार A तथा C के औसत परमाणु भार के लगभग बराबर है। तत्वों की इस प्रकार की व्यवस्था को क्या कहते हैं ? इस प्रकार के तत्वों के समूह का एक उदाहरण दीजिए।
उत्तर– तत्वों की इस व्यवस्था को डोबेरेनर त्रिक कहते हैं। इस प्रकार के तत्वों का समूह है– लीथियम, सोडियम एवं पोटाशियम।
प्रश्न 28. तत्वों को बढ़ते हुए परमाणु द्रव्यमान के क्रम में निम्नलिखित प्रकार से व्यवस्थित किया गया है–
F, Na, Mg, Al, Si, P, S, Cl, Ar, K
(a) समान गुणों वाले तत्वों के दो समुच्चय चुनिए।
(b) उपरोक्त दिया हुआ प्रदर्शन तत्वों के वर्गीकरण के किस नियम से संबंधित है।
उत्तर—
(a) समान गुणों वाले तत्वों के दो समुच्चय हैं–
(i) F, Cl
(ii) Na, K
प्रश्न 29. तत्वों के निम्नलिखित समूहों को कया डॉबेराइनर त्रिक में वर्गीकृत किया जा सकता है?
(a) Na, Si, Cl
(b) Be, Mg, Ca
Be का परमाणु भार 9; Na का 23; Mg का 24; Si का 28; Cl का 35; Ca का 40 है। कारण देकर समझाइये।
उत्तर– (a) Si का परमाणु भार Na एवं Cl के परमाणु भार औसत मान के बराबर है परन्तु इनके गुण भिन्न-भिन्न है। अतः ये डॉबेरेनर त्रिक नहीं बनाते।
(b) Mg का परमाणु भार Be एवं Ca के परमाणु भार के औसत मान के बराबर है तथा इनके गुण भी समान है। अत: ये डॉबेरेनर त्रिक बनाते हैं ।
प्रश्न 30. में डेलीफ आवर्त सारणी में तत्वों को परमाणु भारों के बढ़ते क्रम में व्यवस्थित किया गया है तथा कोबाल्ट परमाणु भार 58.93 शाप को निकल, परमाणु भार 58.71 amu से पहले रखा गया है। इसका कारण दीजिए।
उत्तर– कोबाल्ट एवं निकेल के रासायनिक गुणों के आधार पर कोबाल्ट का परमाणु भार अधिक होने के बावजूद भी मेंडेलीफ ने उसे आवर्त सारणी में निकेल से पहले ‘रखा।
प्रश्न 31. ” आधुनिक आवर्त सारणी में हाइड्रोजन एक अद्वितीय स्थान रखता है।” इस ‘कथन की पुष्टि कीजिए।
उत्तर– हाइड्रोजन एक गैस है जिसका गुण है लोजन से मिलता है, परन्तु इसकी संयोजकता 1 है जो क्षारीय धातुओं के गुणों से मिलता है। अत: हाइड्रोजन को आधुनिक आवर्त सारणी में अद्वितीय स्थान मिला है।
प्रश्न 32. मेंडेलीफ द्वारा पूर्वानुमानित तत्व ‘एका-सिलिकन‘ तथा ‘एका ऐलुमिनियम‘ के क्लोराइडों के सूत्र लिखिए।
उत्तर– एका-सिलिकन– जर्मेनियम का क्लोराइड GeCl3
एका-एल्युमिनियम– गैलियम का क्लोराइड GeCl4
प्रश्न 33. तीन तत्व A, B तथा C के बाहातम कोशों में क्रमश: 3, 4 तथा 2 इलेक्ट्रॉन हैं। आधुनिक आवर्त सारणी में ये तत्व किस समूह संख्या से संबंधित हैं। इनकी संयोजकताएँ भी दीजिए।
उत्तर–
प्रश्न 34. यदि एक तत्व X, समूह 14 में रखा गया है, उसके क्लोराइड का सूत्र क्या होगा तथा बंधन की प्रकृति क्या होगी ?
उत्तर– समूह 14 में रखे सभी तत्वों के वाहयतम कक्षा में 4 इलेक्ट्रॉन होते हैं जो अपना अष्टक पूरा करने के लिए अपने सभी 4 इलेक्ट्रॉनों का साक्षा करके अन्य तत्वों से सहसंयोजक बंध बनाते हैं।
उदाहरण– कार्बन अपने चारों इलेक्ट्रॉनों का क्लोरीन के चार परमाणुओं से साझा कर सहसंयोजक बंध बनाता है।
अत: कार्बन के क्लोराइड का सूत्र है—CCl4 बंध की प्रकृति– सहसंयोजक बंध
प्रश्न 35. दो स्पीशीज X तथा Y की त्रिज्या की तुलना कीजिए। अपने उत्तर का ‘कारण दीजिए। दिया गया है—
(a) X में 12 प्रोटोन तथा 12 इलेक्ट्रॉन हैं
(b) Y में 12 प्रोटोन तथा 12 इलेक्ट्रॉन हैं।
उत्तर-
अत: तत्व X की त्रिज्या Y की त्रिज्या से बड़ी है।
प्रश्न 36. निम्नलिखित तत्वों को परमाण्वीय त्रिज्या के बढ़ते हुए क्रम में व्यवस्थित ‘कीजिए।
(व) Li, Be, F, N
(७) Cl, At, Br, l
उत्तर– (a) F < N < B < Li
(b) Cl < Br < I < At
प्रश्न 37. निम्नलिखित तत्वों, जिनके इलेक्ट्रॉनिक विन्यास नीचे दिए गए हैं, में धातुओं को पहचानिए एवं उनके नाम दीजिए।
(a) 2, 8, 2
(b) 2, 8, 1
(c) 2, 8, 7
(d) 2, 1
उत्तर- (a) दिए गए तत्व का इलेक्ट्रॉनिक विन्यास 2, 8, 2 है जिसका कुल इलेक्ट्रॉनों की संख्या 12 है। अत: यह तत्व मैग्नीशियम ( Mg) है।
(b) तत्व का इलेक्ट्रॉनिक विन्यास 2, 8, 1 है। इसके कुल इलेक्ट्रॉन संख्या । है। अत: यह सोडियम (11) है।
(c) तत्व का इलेक्ट्रॉनिक विन्यास 2, 8, 7 है। इसके कुल इलेक्ट्रॉन 17 है। अत: यह क्लोरोन (Cl) गैस है।
(d) तत्व का इलेक्ट्रॉनिक विन्यास 2, । है। इसके कुल 3 इलेक्ट्रॉन है। अत: यह लीथियम (Li) है।
प्रश्न 38. तत्व A ( परमाणु क्रमांक 19 ) जब तत्व B ( परमाणु क्रमांक 17 ) से संयोग करता है तो बनने वाले उत्पाद का सूत्र लिखिए। इसका इलेक्ट्रॉनिक बिंदु सूत्र बनाइये। बनने वाले बंध की प्रकृति कया है?
उत्तर- तत्व A का इलेक्ट्रॉनिक विन्यास-
A19 → 2, 8, 8, 1
इसकी संयोजकता इलेक्ट्रॉन 1 है।
तत्व B का इलेक्ट्रॉनिक विन्यास-
B 17 2, 8, 7
इसकी संयोजकता इलेक्ट्रॉन 7 है।
अत: तत्व A अपना 1 इलेक्ट्रॉन त्यागकर तत्व B के साथ आयनिक बंध बनाता है।
बंध की प्रकृति → आयनिक बंध
प्रश्न 39. निम्नलिखित तत्वों को उनके धात्विक गुणों के बढ़ते हुए क्रम में व्यवस्थित ‘कीजिए।
Mg, Ca, K, Ge, Ga
उत्तर- Ge < Ga < Mg < Ca < K
प्रश्न 40. निम्नलिखित गुणों के आधार पर तत्वों को पहचानिए तथा उन्हें सक्रियता के बढ़ते हुए क्रम में व्यवस्थित कीजिए।
(a) एक तत्व जो मुलायम है तथा सक्रिय धातु है।
(b) एक धातु जो चूना पत्थर का महत्वपूर्ण अवयव है।
(c) वह धातु जो कक्ष ताप पर द्रव अवस्था में रहता है।
उत्तर- (a) सक्रिय धातु Na
(b) चूना पत्थर का महत्वपूर्ण अवयव Ca
(c) कक्ष ताप पर द्रव अवस्था में धातु झट सक्रियता का बढ़ता क्रम Hg < Ca < Na
प्रश्न 41. तत्वों के गुण नीचे दिए गए हैं। आवर्त सारणी में आप इन तत्वों को कहाँ पायेंगे ?
(a) एक मुलायम धातु जिसे किरोसिन में संग्रहित किया जाता है।
(b) परिवर्तनशील (एक से अधिक) संयोजकता युक्त एक तत्व जिसे जल में संग्रहित किया जाता है।
(c) एक तत्व जो चतु: संयोजी है तथा कार्बनिक रसायन का आधार है।
(d) परमाणु क्रमांक 2 वाला तत्व, जो एक अक्रिय गैस है।
(e) एक तत्व जिसकी पतली ऑक्साइड परत अन्य तत्वों को ‘ ऐनोडीकरण‘ प्रक्रम में द्वारा संक्षारण प्रतिरोधी बनाती है।
उत्तर-
(a) सोडियम (Na) — समूह 1, आवर्त 3
(b) फॉस्फोरस (P) — समूह 15, आवर्त 3
(c) कार्बन (C) — समूह 14, आवर्त 2
(d) हीलियम (He) — समूह 18, आवर्त 1
(e) एल्युमीनियम (Al)— समूह 13, आवर्त 3
दीर्घउत्तरीय प्रश्न
प्रश्न 42. एक तत्व को आवर्त सारणी के दूसरे समूह तथा तृतीय आवर्त में रखा गया है। ऑक्सीजन की उपस्थिति में दहन पर यह क्षारीय ऑक्साइड देता है।
(a) तत्व को पहचानिए।
(b) इस तत्व का इलेक्ट्रॉनिक विन्यास लिखिए ।
(c) जब इसे वायु की उपस्थिति में जलाया जाता है तो अभिक्रिया की संतुलित रासायनिक समीकरण दीजिए।
(d) इस ऑक्साइड को जल में घोला जाता है तो प्रक्रिया की संतुलित रासायनिक समीकरण दीजिए।
(e) इस ऑक्साइड के लिए इलेक्ट्रॉन बिन्दु संरचना बनाइये।
उत्तर- (a) मैग्नीशियम (Mg)
(b) तत्व का इलेक्ट्रॉनिक विन्यास
प्रश्न 43. एक तत्व X ( परमाणु क्रमांक 17 ) एक अन्य तत्व Y ( परमाणु क्रमांक 20 ) से अभिक्रिया कर द्वि-संयोजी हैलाइड बनता है।
(a) आवर्त सारणी में तत्व X तथा Y को कहाँ रखा गया है?
(b) X तथा Y को धातु, अधातु अथवा उपधातु के रूप में वर्गीकृत कीजिए।
(c) तत्व Y के ऑक्साइड की प्रकृति क्या होगी ? निर्मित यौगिक में बंधन की प्रकृति को पहचानिए।
(d) इसके द्वि-संयोजी हैलाइड की इलेक्ट्रॉन बिंदु संरचना बनाइये।
उत्तर– तत्व X का परमाणु क्रमांक 17
अत: X17 → 2, 8, 7
तत्व Y का परमाणु क्रमांक 20
अत: Y20 → 2, 8, 8, 2
(a) आवर्त सारणी में तत्व X का स्थान समूह 17, आवर्त 3
तत्व Y का स्थान समूह 2, आवर्त 4
(b) तत्व झट अधातु है।
तत्व Y धातु है।
(c) तत्व Y के ऑक्साइड की प्रकृति क्षारीय है। निर्मित यौगिक में आयनिक बंध है।
(d) द्विसंयोजी हैलाइड कैल्शियम क्लोराइड (CaCl2 ) है। इसकी इलेक्ट्रॉन बिंदु संरचना-
प्रश्न 44. कुछ तत्वों के परमाणु क्रमांक नीचे दिए गए हैं–
10, 20, 7, 14
(a) तत्वों को पहचानिए।
(b) आवर्त सारणी में इन तत्वों की समूह संख्या पहचानिए।
(c) आवर्त सारणी में इन तत्वों के आवर्त पहचानिए।
(d) प्रत्येक तत्व का इलेक्ट्रॉनिक विन्यास कया होगा ?
(e) इन तत्वों की संयोजकता निर्धारित कीजिए।
उत्तर- दिए गए तत्वों के परमाणु क्रमांक
10, 20, 7, 14
(a) परमाणु क्रमांक 10 वाले तत्व नियॉन (Ne) है।
(b) परमाणु क्रमांक 20 वाले तत्व कैल्शियम (Ca) है।
(c) परमाणु क्रमांक 7 वाले तत्व नाइट्रोजन (N) है।
(d) तत्वों के इलेक्ट्रॉनिक विन्यास–
2, 8; 2, 8, 8, 2; 2, 5; 2, 8, 4
(e) तत्वों की संयोजकता-
परमाणु क्रमांक 10 संयोजकता 0 (शून्य)
परमाणु क्रमांक 20 संयोजकता 2
परमाणु क्रमांक 7 संयोजकता 3
परमाणु क्रमांक 14 संयोजकता 4
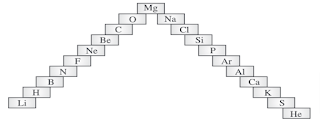
प्रश्न 45. निम्नलिखित वर्ग पहेली ( चित्र 5.1) को अंग्रेज़ी में पूर्ण कीजिए। बायें से दायें
(1) परमाणु क्रमांक 12 वाला तत्व
(2) एक धातु जिसका उपयोग डिब्बे बनाने में होता है तथा समूह 14 का सदस्य है।
(3) एक चमकदार अधातु जिसके बाह्मतम कोश में 7 इलेक्ट्रॉन होते हैं।
उत्तर-
ऊपर से नीचे
(5) अत्यधिक क्रियाशील एवं मुलायम धातु जो ज्वाला के संपर्क में लाने पर उसे पीला रंग प्रदान करती है तथा जिसे किरोसिन में रखा जाता है।
(6) द्वितीय आवर्त का प्रथम तत्व।
(7) एक तत्व जिसका उपयोग प्रतिदीप्ती बल्ब बनाने में होता है तथा जो आधुनिक आवर्त सारणी के समूह 18 का द्वितीय सदस्य है।
(8) एक रेडियो सक्रिय तत्व जो हैलोजन परिवार का अंतिम सदस्य है।
(9) धातु जो कि स्टील का प्रमुख अवयव है तथा नम वायु में उदभासन पर जंग बनता है।
(10) आधुनिक आवर्त सारणी का प्रथम उपधातु जिसके रेशों का उपयोग बुलेटप्रूफ जैकेट बनाने में होता है।
प्रश्न 46. (a) इस सीढ़ी में तत्वों के संकेत अस्तव्यस्त करके लिख दिए गए हैं। तत्वों के इन संकेतों को आवर्त सारणी में परमाणु क्रमांक के बढ़ते हुए क्रम में पुनर्व्यवस्थित कीजिए ।
(b) इनको समूहों के क्रम में भी व्यवस्थित कीजिए ।
उत्तर- (a) तत्वों के परमाणु क्रमांक के बढ़ते हुए क्रम-
H < He < Li < Be < B < C < N < O < F < Ne < Na < Mg < Al < Si < P < S < Cl < Ar < K < Ca
(b) समूह 1 – H, Li, Na, K
समूह 2 – Be, Mg, Ca
समूह 13 – B, Al
समूह 14 – C, Si
समूह 15 – N, P
समूह 16 – O, S
समूह 17 –F, Cl
समूह 18 – He, Ne, Ar
प्रश्न 47. मेंडेलीफ ने कुछ तत्व जो उस समय ज्ञात नहीं थे के अस्तित्व का अनुमान लगाया तथा उनमें से दो तत्वों को ‘एका-सिलिकन‘ तथा ‘ एका-ऐलुमिनियम ‘ नाम दिया।
(a) उन तत्वों के नाम दीजिए जिन्होंने इन तत्वों का स्थान लिया।
(b) आवर्त सारणी में इन तत्वों के समूह तथा आवर्त बताइये।
(c) इन तत्वों को धातु, अधातु अथवा उपधातु के रूप में वर्गीकृत कीजिए।
(d) इनमें से प्रत्येक में कितने सहसंयोजी इलेक्ट्रॉन उपस्थित है।
उत्तर- (a) एका-सिलिकन—जर्मेनियम
एका-एल्युमिनियम — गैलियम
(b) जर्मेनियम → समूह 14 आवर्त 4
गैलियम → समूह 13 आवर्त 4
(c) जर्मेनियम — उपधातु
गैलियम— धातु
(d) जर्मेनियम → संयोजकता इलेक्ट्रॉन 4
गैलियम → संयोजकता इलेक्ट्रॉन 3
प्रश्न 48. (a) तत्वों का धनविद्युती गुण समूह में नीचे जाने पर बढ़ता है तथा आवर्त में बायें से दायें जाने पर घटता है।
(b) तत्वों की विद्युतऋणता समूह में नीचे जाने पर घटती है तथा आवर्त में बायें से दायें जाने पर बढ़ती है।
(c) परमाणु त्रिज्या समूह में नीचे जाने पर बढ़ती है तथा आवर्त में बायें से दायें जाने पर घटती है।
(d) धात्विक गुण समूह में नीचे जाने पर बढ़ता है तथा आवर्त में बायें से दायें जाने पर घटता है।
उपरोक्त प्रवृत्तियों के आधार पर आवर्त सारणी में 3 से 9 परमाणु क्रमांक बाले तत्वों के लिए निम्नलिखित के उत्तर दीजिए।
(a) इनमें से सबसे अधिक धनविद्युती तत्व का नाम दीजिए।
(b) सबसे अधिक ऋणविद्युती तत्व का नाम दीजिए।
(c) सबसे छोटे परमाण्वीय आकार वाले तत्व का नाम दीजिए।
(d) उस तत्व का नाम दीजिए जो उपधातु है।
(e) उस तत्व का नाम दीजिए जो अधिकतम संयोजकता प्रदर्शित करता है।
उत्तर- (a) लिधियम, (b) फ्लोरीन, (c) फ्लोरीन, (d) बोरॉन, (e) कार्बन
प्रश्न 49. एक तत्व X जो कक्ष ताप पर पीला ठोस है श्रृंखलन तथा अपररूपता दर्शाता है। X दो प्रकार के ऑक्साइड बनाता है जो कि फैरस सल्फेट क्रिस्टल के तापीय विघटन के दौरान भी बनते हैं तथा प्रमुख वायु प्रदूषक हैं ।
(a) तत्व हू को पहचानिए।
(b) ऊ का इलेक्ट्रॉनिक विन्यास लिखिए ।
(c) फैरस सल्फेट क्रिस्टल के तापीय अपघटन की संतुलित रासायनिक समीकरण लिखिए।
(d) बनने वाले ऑक्साइड की प्रकृति ( अम्लीय/क्षारकीय) कया होगी ?
(e) आधुनिक आवर्त सारणी में तत्व की स्थिति बताइये।
उत्तर- (a) तत्व X → सल्फर (S)
(b) K (2), L(8), M (6)
(e) आवर्त 3 समूह 16
प्रश्न 50. समूह 5 का एक तत्व X द्वि-परमाण्वीय अणु के रूप में रहता है तथा उत्प्ररक की उपस्थिति में 773 K पर हाइड्रोजन से संयोग पर एक यौगिक, अमोनिया बनता है जिसकी अभिलक्षणिक तीक्षण अरुचिकर गंध होती है।
(a) तत्व X को पहचानिए। यह कितने संयोजी इलेक्ट्रॉन रखता है।
(b) X के द्वि-परमाण्वीय अणु की इलेक्ट्रॉन बिंदु संरचना बनाइये। इसमें किस प्रकार का बंध बनता है।
(c) अमोनिया की इलेक्ट्रॉन बिंदु संरचना बनाइये। इसमें किस प्रकार के बंध बनते हैं ?
उत्तर- (a) तत्व X नाइट्रोजन (N) है। इसकी संयोजी इलेक्ट्रॉनों की संख्या 5 है।
प्रश्न 57. मेंडेलीफ की आवर्त सारणी में किस समूह के तत्वों को बिना मूल क्रम में परिवर्तन किए रखा जा सकता है, कारण दीजिए।
उत्तर- उत्कृष्ट गैसों का समूह मेंडेलीफ की आवर्त सारणी में तत्वों के गुण उनके परमाणु द्रव्यमान के आवर्ती फलन होते हैं ।
प्रश्न 52. तत्वों के वर्गीकरण के लिए मेंडेलीफ द्वारा अपनाए गए प्रक़रम को बताइये। वे आवर्त नियम तक किस प्रकार पहुँचे ?
उत्तर- उत्तर के लिए मेंडेलीफ की आवर्त सारणी के नियम देखें ।